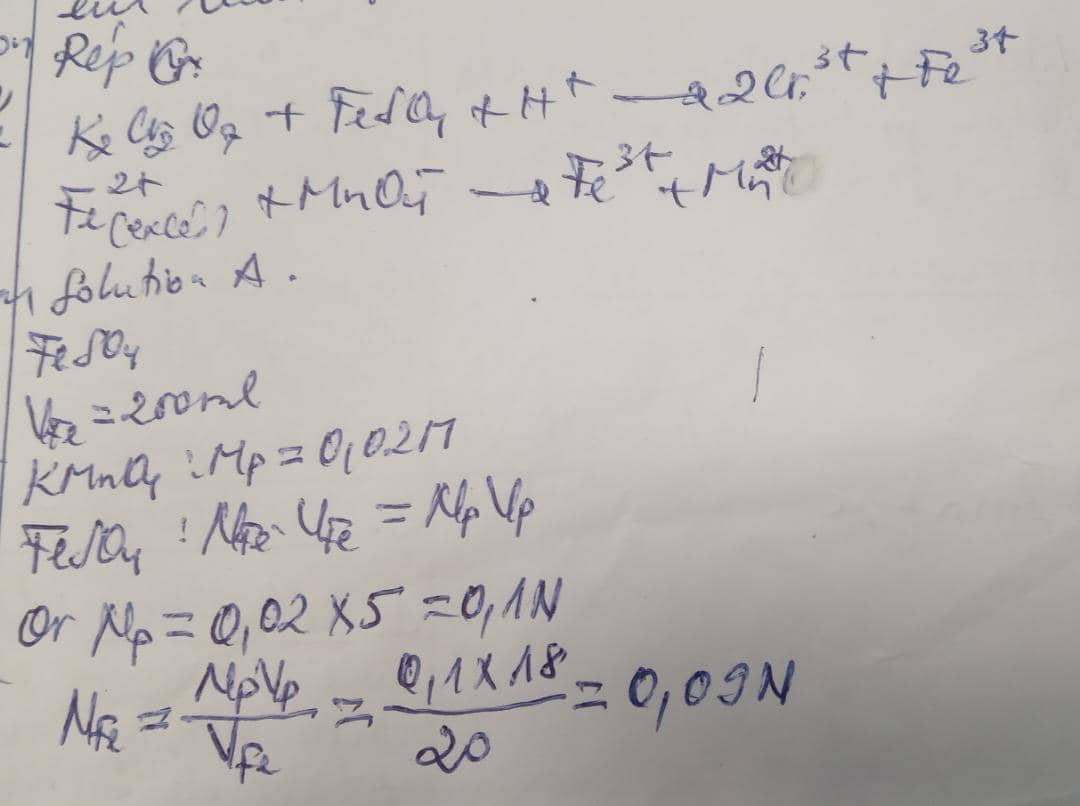a) Révision: On trouve 0,2g de pyrolusite (dioxgde dimangoinèse) par 25 ml d'une solution de Hcl à 37% et on recueille le chlore qui se dégage dans une solution de KI à 2%.On titre l'iodeliberé par la réaction au thiosalfate de sodium 0,1N.On utilise à cet effet 38,2ml.Quel est le titre en dioxyole de manganèse dans pyrolusite?
b) Motivation: Dans quelle reaction peut-on trouver Cr2O72- + 6e- +14H+ ----> 2Cr3+2 + 7H2o?
c) Annonce
Qu'est-ce que nous allons étudier aujourd'hui?
II. Analyse
Quels sont les avantages de le bichromotométrie?
Quels sont les inconcenients de le Bichromatemetrie?
Exemple: Dans 200ml d'une solution de bichromate de potassium, on verse 40ml de solution A de sulfate de Fer (II), la solution obtenue est verdoitre; elle vire au rose persistante par addition de 7,2ml d'une solution de KmrO4 0,02M. Calculer la concentration de la solution (N,M et g/l) de bichromate sachant que 20ml de A vire au rose persistante par addition de 18ml de la solution de KmrO4.
Quelles sont les méthodes d'argentimetrie?
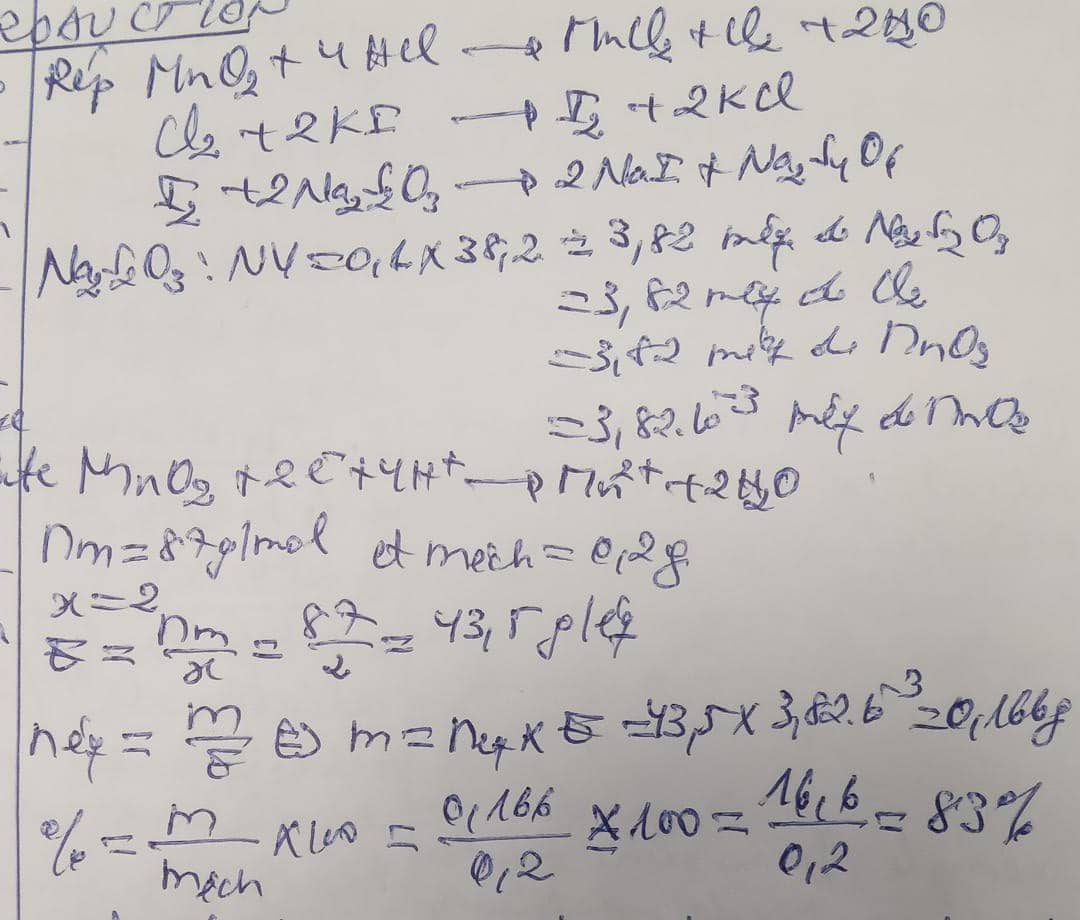
C'est une réaction bichromatométrique.
Aujourd'hui nous allons parlé de dosage bichromatométrique.
3. BICHROMATOMETRIE OU BICHROMATOMETRIQUE
1.Le principe de la bichromatométrie est le dosage des réducteurs par le K2Cr2 O7. Quel mot est dérivé du verbe s'exercer ? Le mot qui est dérivé du verbe s'exercer est l'exercice.
2. L'indication de fin de titrage: on utilise la diphenylamine sulforée (C6H5)2 et Ferriganure de potassium K4[ Fe (CN)6] qui virent dans l'incobre au violet.
3.Milieu réactionnel: la Bichromatométrie utilise preferentiellement l'acide sulfunique (H2SO4)dilué.
4. Avantage et inconvénients
a) Avantage :
*Le K2Cr2 O7 en solution acquieuse est très stable et il n'est pas sensible à la choleur et la lumière.
* le K2Cr2 O7 permet de preparer directement des solutions titrées.
* On peut effectuer les dosages en présences de Hcl concentré ou doser les chlorures métallique.
b) Inconvénient :
*le K2Cr2 O7 est un oxydant mois fort que le KMnO4.
* Le K2Cr2 O7 est un système lent en milieu alcalin Cr3t / Cr.O2-4.
* le K2Cr2 O7 est donc un pseudo-indicateur redox interne.