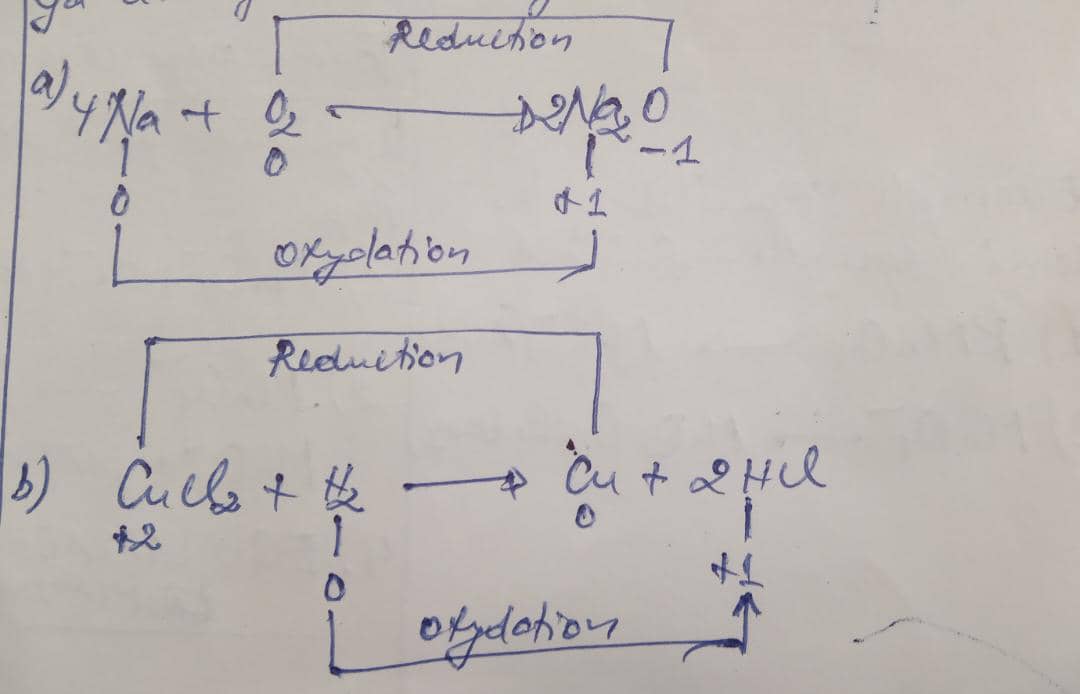
a) Révision:
Qu'entendez-vous par : 1) Une Oxydation?; 2) une réduction?
b) Motivation: Comment appel-t-on deux phenomèns simultanés et inverse ?
c) Annonce du sujet:
Nous allons étudier quoi aujourd'hui ?
II. Analyse
Exemples: Equilibrez les demi-équation redox suivants:
2) Equilibrez les demi-équation suivant
3) Chercher les coéfficients de la réaction suivante : KBr + KMnO4 + H2SO ---> Br2 + nrSO4 + K2SO4 + H2O
a) 10|2|8|| 5| 2|2|6|8
b) 5|1|4||5|1|3|4
c)5|1|4||5|1|3|4
d) 6|1|4|6||1|3|4
e) 5|2|8||5|2|6|8.
1) Une reduction est une montée d'E.O par perte d'élections.
2) Une Réduction est une descente d'E.O par gain d'élections
c'est une Oxydation et Réduction.
Aujourd'hui nous allons parlé de l'oxydation et réduction.
2. OXYDATION & REDUCTION
L'oxydation et réduction sont deux phenomenes simultané et inversé.
2.1. Définition: Une réaction d'oxyda-réduction ou Reddox est une réaction dans la quelle il y à la fois une oxydation et une réduction.