

A. REVISION
Quel est le niveau d'énergie atteind par l'électron si nous lui fournissons une énergie correspondant à 99% du potentiel d'ionisation?
B. MOTIVATION
Comment se trouve les électrons sur une couche atomique?
C. ANNONCE DU SUJET
A. ANALYSE
Qu'est ce qu'on fait pour décrire une orbite?
Quelles sont les caractéristiques des orbites elliptiques stationnaires?
Qu'entendez-vous par le nombre quantique principales?

Les électrons sur une couche atomique sE présentent sous forme des orbites elliptiques
LES ORBITES ELLIPTIQUES DES SOMMERFELD
D'après BOHN, l'électron circule sur une orbite circulaire et les charges sont considérées comme ponctuelles.
Si bien que le champs électronique est uniquement un champ colombien.
SOMMERFELD suggéra l'existence d'orbite elliptique stable avec le noyau comme foyer, en plus d'orbites circulaires pour l'électron.
Les orbites elliptiques possible sont celles dont le petit axe est un multiple entier du noyau unitaire. Pour expliciter la configuration atomique, il faudra donc deux paramètre ou nombre quantique.
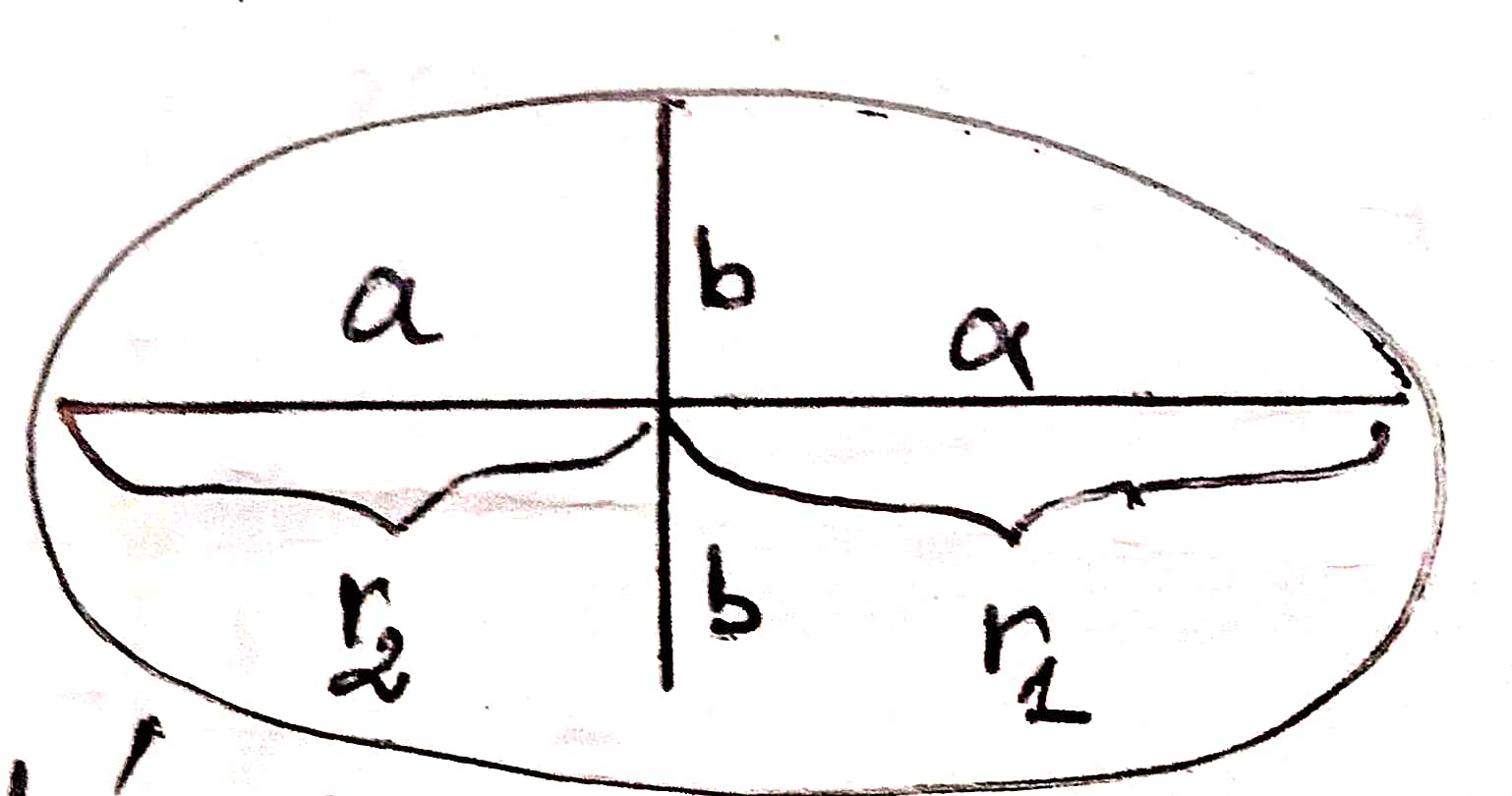
n=nombre quantique principal représente le grand axe
k=nombre quantique azimutal représente le petit axe
a) pour décrire une orbite elliptique stationnaire, l'électron doit satisfaire à la condition:
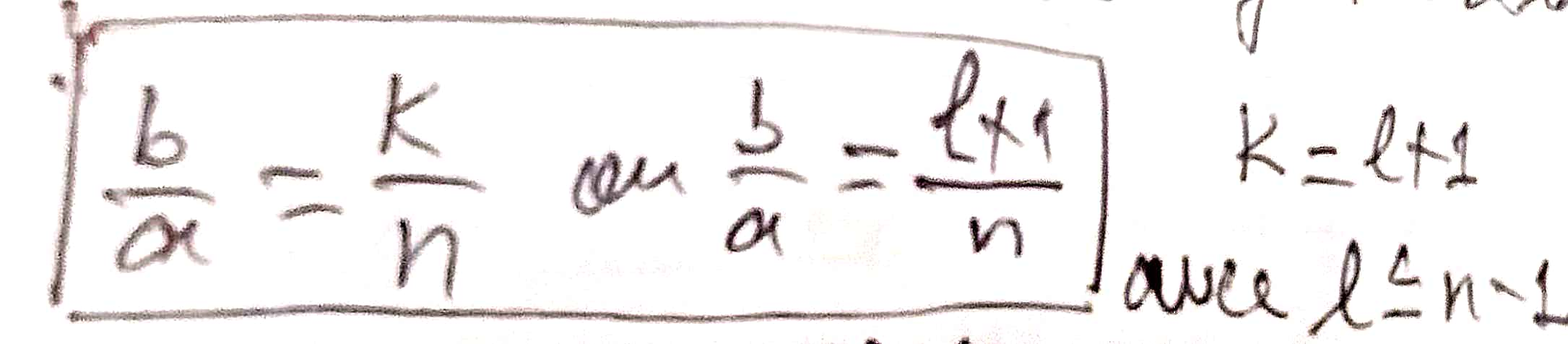
a=demi grand axe de l'ellipse
b=demi petit axe de l'ellipse
l=nombre quantique secondaire
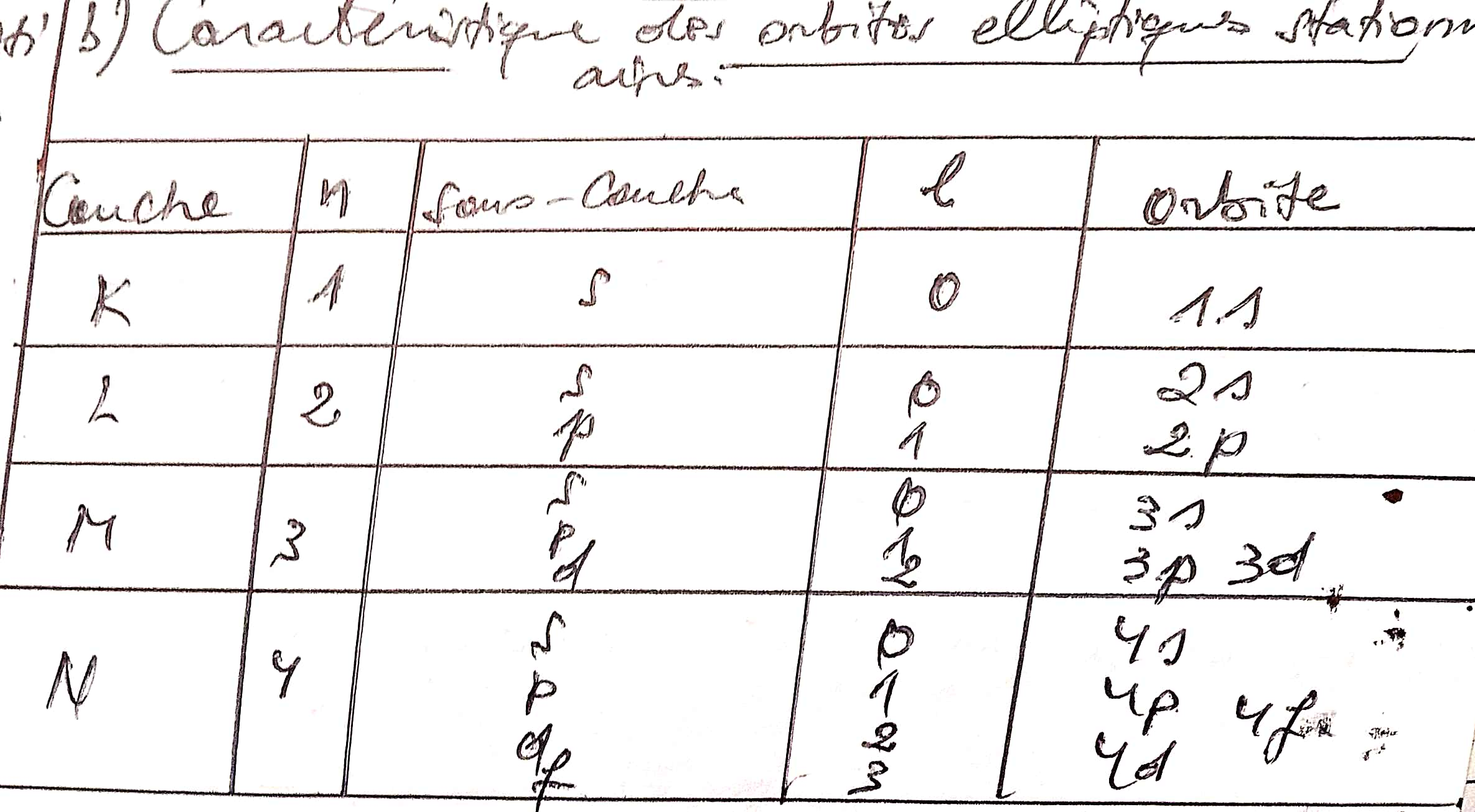
CARACTERISTIQUES DES ORBITES ELLIPTIQUES STATIONNAIRES
NOMBRE QUANTIQUE
Les nombres(n, l, m, et s) sont dont quantiques parce qu'ils ne peuvent prendre qu'un certain nombre de valeurs permises
NOMBRE QUANTIQUE PRINCIPPALE(N)
Ce nombre indique le numéro d'ordre de l'orbite sur lequel se trouve effectivement l'électron et donne la dimension de l'orbite.
-Ce nombre indique le numéro d'ordre
-Ce nombre décrit la taille de l'orbite cad la distance entre l'électron et le noyau
-Ce nombre quantique ne peut prendre que des valeurs positives:
n=1, 2, 3, 4, 5, 6, 7 ces sont donc les numéros

NOMBRE QUANTIQUE SECONDAIRE (L)
-Ce nombre détermine la forme de l'orbite où il décrit la géométrie du nuage électronique
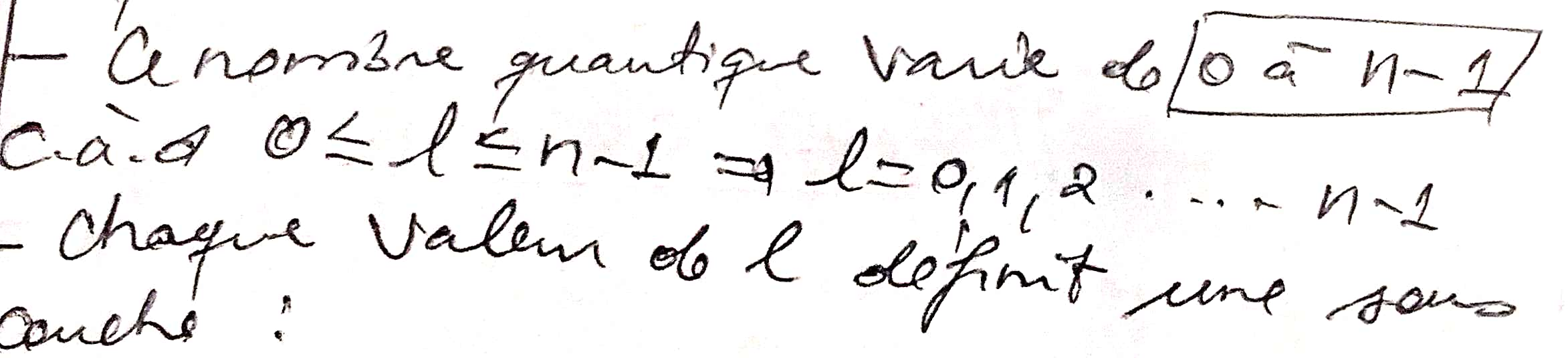
l=0, on a la sous-couche s(scharp)
l=1, on a la sous-couche p(principale)
l=2, on a la sous-couche d(diffuse)
l=3, on a la sous couche f(fondamentale)
-Chaque valeur de L correspond à une forme d'orbite
-Ce nombre quantique est donné par m=(2l +1) valeur ou m=2n-1
n=m+1/2
NOMBRE QUANTIQUE DE SPION (A ou As ou S)
Il désigne la rotation de l'électron sur lui-même.
Ce nombre quantique peut prendre la valeur de +1/2 ou de -1/2, la valeur de Ms ne dépend donc pas des trois autres nombres quantiques.
NB: lorsque la rotation à eu lieu dans le même sens que ses déplacements sur orbite, le spin est positif, il est négatif dans le sens contraire. A chaque orbite permise corresponds deux spins:
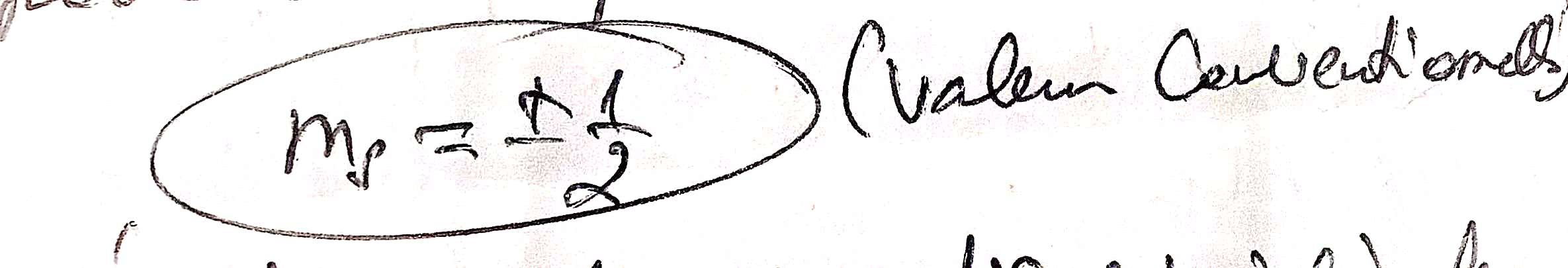
n= représente le nombre quantique principale
l=représente le nombre quantique secondaire
m=nombre quantique magnétique
s=nombre quantique de spin