II. DEVELOPPEMENT
ANALYSE(SUITE)
Qu'entendez-vous par l'oxydant et réducteur conjugués?
Comment se présente le couple redox?
C'est quoi le potentiel redox?
Qu'entendez-vous par l'électrode à Hydrogène normale?
II. DEVELOPPEMENT
ANALYSE(SUITE)
3. OXYDANT ET REDUCTEUR CONJUGUES
La forme oxydée et réduite d'un couple redox présentent des tendances opposées qu'on peut traduire par une demi-équation réversible.
Forme oxydée - ne- vers Forme réduite
Couple redox :
Ce4+ / Ce3+
MnO-4 / Mn2+
Cr2Ov7 / V3+.
4. POTENTIEL REDOX
A cause d'une différence de potentiel entre un oxydant et réducteur, les électrons se déplacent et occasionnent un courant électrique.
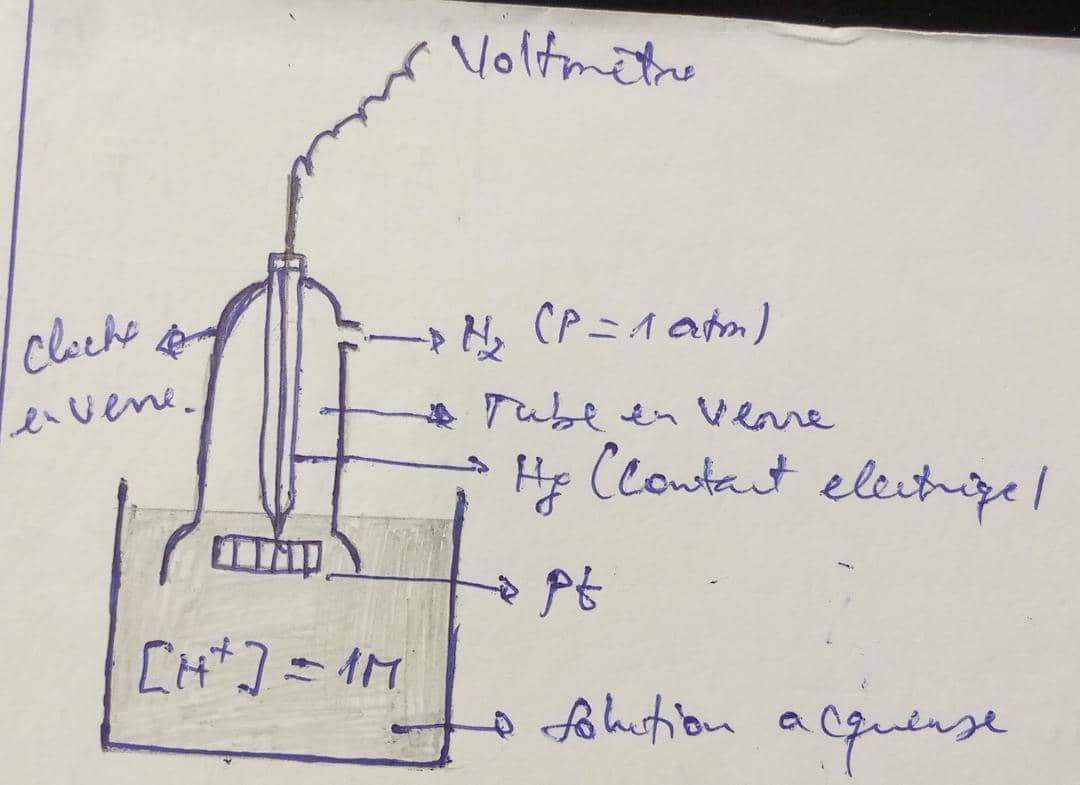
1° Electrode à Hydrogène normale
Il s'agit d'une solution d'ions H+ à la concentration 1M (pH=), saturée d'Hydrogène gazeux (H2) à la pression de 1 atmosphère (P = 10m)
Dans cette solution plonge une électrode de platine recouvert de noir de platine.