

A. RAPPEL
Qu'aviez vous vu hier?
Nous avons combien de types d'électrolyse?
B. MOTIVATION
De quelle façon pouvons nous distinguer l'électrolyse?
C. ANNONCE
Nous étudions la classification des électrolyses
Montrez le tableau de l'électrolyse fort et faible.
Quelle est l'importance de l'eau et donner sa formule?
Pourquoi l'ion hydrogène est H+ ?
Qu'est-ce qui se passe en solution acqueuse?
La température de l'eau varie en combien de degré?
Calculez la constante d'acedité du sul fate d'hydrogène sachant que 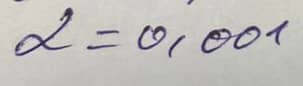 en solution M/20
en solution M/20
Calculez le degré d'ionisation cyanure d'hydrogène (HCN) en solution n, 0,1 tandis que Ki est 7.10-2
Hier nous avions vu l'électrolyse
Nous avons deux types d'électrolyses
CLASSIFICATION DES ELECTROLYSES FORTS ET FAIBLE
ELECTROLYSE FORT
| Acide | Base | Sels |
|---|---|---|
|
Hcl, HI HDH,H2 SO4 H NO3 LHCPO4 H2S2O4 Hmn O4 HCPO4 |
Na OH, Si OH KO HICSOH Ca (OH)2 Ba (OH)2 (SOH) Mg (OH)2 |
Tous les sels sont soluble |
| ACIDE | BASE | SELS |
|---|---|---|
|
H+U2 Si HCM HNO2,H2 SO3 HCLO H2 LO3 |
NH HOHO mi pricsiomiline hydrolydes autres que greux former par le metaux elles familles |
eau pure |
L'importance de l'eau
Elle apporte les nutriments essentiels au bon fonctionnement du corps humain, régule notre température, favorise l'élimination des déchets et des toxines… l'eau est indispensable à notre santé. D'ailleurs, saviez-vous qu'environ 60 % de notre organisme est composé d'eau ?
La formule chimique de l'eau pure est : H 2 O . Cela signifie que c'est une molécule composée de deux atomes d'hydrogène, liés de manière covalente à un atome d'oxygène.
L'atome d'hydrogène H, de numéro atomique Z = 1, est constitué d'un noyau compor- tant un seul proton et d'un cortège électronique comportant un seul électron. L'ion hydrogène H+ est un atome d'hydrogène qui a perdu un électron, donc un ion hydrogène est un proton.
A pression atmosphérique, l'eau est à l'état liquide entre 0°C et 100°C. En-dessous de 0°C, elle se transforme en glace. En-dessus de 100°C, elle se transforme en vapeur. Dans une installation solaire, l'eau ne bout pas à 100°C, mais à une température supérieure à 120°C.